De samenstelling van het atoom
Uit de evolutie van de atoommodellen is er al gebleken dat een atoom bestaat uit een kern en een mantel.
Een atoom heeft een welbepaalde massa. De massa van een atoom is uiterst klein en is hoofdzakelijk afkomstig van de deeltjes uit de kern, de protonen en de neutronen.
In de mantel bevinden zich de elektronen, de negatief geladen deeltjes. De elektronen hebben ook een massa, maar die is te verwaarlozen ten opzichte van de massa van de kerndeeltjes.
De massa van een proton bedraagt ongeveer 1,6726 . 10-27 kg, de massa van een neutron bedraagt ongeveer evenveel. Omdat de massa van een proton en een neutron en dus van een atoom zo klein is, heeft men voor deze massa’s een nieuwe eenheid gekozen, de unit, met symbool u.
1 u = 1,6605 . 10-27 kg
Een atoom is neutraal: dat wil zeggen dat het aantal positieve ladingen gelijk is aan het aantal negatieve ladingen. Anders gezegd: in een atoom is het aantal protonen gelijk aan het aantal elektronen.
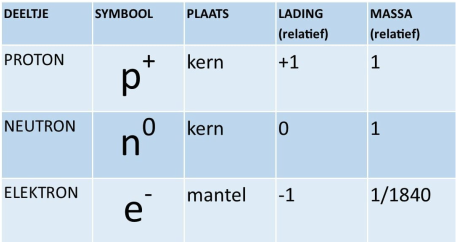
Samengevat:
Uit de evolutie van de atoommodellen is er al gebleken dat een atoom bestaat uit een kern en een mantel.
Een atoom heeft een welbepaalde massa. De massa van een atoom is uiterst klein en is hoofdzakelijk afkomstig van de deeltjes uit de kern, de protonen en de neutronen.
In de mantel bevinden zich de elektronen, de negatief geladen deeltjes. De elektronen hebben ook een massa, maar die is te verwaarlozen ten opzichte van de massa van de kerndeeltjes.
De massa van een proton bedraagt ongeveer 1,6726 . 10-27 kg, de massa van een neutron bedraagt ongeveer evenveel. Omdat de massa van een proton en een neutron en dus van een atoom zo klein is, heeft men voor deze massa’s een nieuwe eenheid gekozen, de unit, met symbool u.
1 u = 1,6605 . 10-27 kg
Een atoom is neutraal: dat wil zeggen dat het aantal positieve ladingen gelijk is aan het aantal negatieve ladingen. Anders gezegd: in een atoom is het aantal protonen gelijk aan het aantal elektronen.
Samengevat:
Atoomnummer (Z)
Het aantal protonen noemen we het atoomnummer Z van het element. Dit getal is specifiek voor een element.
Z = #protonen (p+) = #elektronen (e-)
Massagetal (A)
De massa van het atoom is vrijwel volledig in de kern geconcentreerd. De massa is gelijk aan de som van het aantal protonen en het aantal neutronen.
Z = #protonen + #neutronen (N of n°)
Het aantal protonen noemen we het atoomnummer Z van het element. Dit getal is specifiek voor een element.
Z = #protonen (p+) = #elektronen (e-)
Massagetal (A)
De massa van het atoom is vrijwel volledig in de kern geconcentreerd. De massa is gelijk aan de som van het aantal protonen en het aantal neutronen.
Z = #protonen + #neutronen (N of n°)
Het atoomnummer Z en het massagetal A van een element zijn twee erg belangrijke waarden. Met beide waarden kun je op een eenvoudige manier de samenstelling van elk atoom berekenen. We tonen dat aan met een voorbeeld:
We willen de samenstelling van een atoom Zilver (Ag) berekenen:
Ag
Z=47
A=108
Het aantal protonen wordt weergegeven door het atoomnummer:
Z=47= aantal protonen
Een atoom is neutraal, dus is het aantal prtonen gelijk aan het aantal elektronen:
#p+ = #e- = 47
We weten dat
A = Z+N
Daaruit leiden we af dat
N=A-Z = 108-47 = 61 = aantal neutronen (# n°)